ANM a inclus Zolgensma în lista de medicamente gratuite şi compensate
ANM a inclus Zolgensma în lista de medicamente gratuite şi compensate
Facebook Twitter Whatsapp Linkedin PinterestExperţii Agenţiei Naţionale a Medicamentului au aprobat la sfârşitul lunii noiembrie a anului trecut medicamentul Zolgensma, o terapie genică destinată pacienţilor care suferă de amiotrofie spinală, o boală genetică gravă care duce la atrofierea muşchilor.
Terapia are rol important în stagnarea bolii şi redarea mobilităţii pacienţilor, conform medicilor care au administrat-o deja. Practic, decizia de includere a acestei terapii în lista de medicamente gratuite şi compensate de care beneficiază asiguraţii a fost luată de ANM, în funcţie de nişte punctaje care ţin cont inclusiv de nivelul de eficienţă şi siguranţă al medicamentului. Terapia genică Zolgensma este la ora actuală cel mai scump tratament din lume. Răzvan Mihai Prisada, preşedintele ANM a precizat pentru News.ro că mai sunt câţiva paşi pentru ca acest medicament să poată ajunge efectiv la pacienţi.
În acest moment, în România părinţii copiilor diagnosticaţi cu această afecţiune strâng aceste sume enorme cu ajutorul organizaţiilor non guvernamentale. Foarte puţini dintre ei sunt aleşi în cadrul unei tombole organizate de compania producătoare, prin care efectiv sunt extrase aleator numele unor copii eligibili, din toată lumea, în limita a 100 de tratamente puse la dispoziţie gratuit. În acest moment, medicamentul este decontat de stat în 8 ţări europene. La ultima actualizare a listei de medicamente gratuite şi compensate, care a avut loc la sfârşitul lunii martie din iniţiativa Ministerului Sănătăţii, această nouă terapie nu a fost inclusă, scrie stiripesurse.ro.
„La Agenţia Medicamentului a fost evaluată în cadrul Direcţiei Evaluare Tehnologii medicale aplicaţia pentru medicamentul Zolgensma şi a fost emisă la sfârşitul lunii noiembrie a anului trecut o decizie de includere necondiţionată, cu anumite observaţii, care este practic prima etapă şi cea care ţine de Agenţia Naţională a Medicamentului în ceea ce priveşte evaluarea unui produs nou care urmează a fi intrat în piaţă, aceasta este partea care a fost deja realizată.
Etapele următoare procedurale sunt introducerea medicamentelor noi, inclusiv acesta, în completarea Hotărârii de Guvern 720/2008, este Hotărârea de Guvern care cuprinde denumirile comune internaţionale corespunzătoare medicamentelor de care beneficiază asiguraţii, pe bază de prescripţie medicală, şi cu o a treia etapă, ulterior acestui moment, va fi necesitatea elaborării protocoalelor terapeutice corespunzătoare, de către Comisiile de Specialitate ale Ministerului Sănătăţii.
ANM a evaluat dosarul medicamentului Zolgensma în baza unei proceduri de lucru şi de acordare a unui punctaj, punctaj care se acordă prin referenţiere la 3 Agenţii ale Medicamentului din Germania, Franţa şi Marea Britanie, există acolo o procedură pe baza căreia acel punctaj dă o rezoluţie privind includerea necondiţionată, includerea condiţionată, adică aşa numitele contracte cost volum sau neincluderea atunci când punctajul nu este suficient, procedura este aplicabilă tuturor medicamentelor noi care vin pentru evaluare.
Este o intrare în lista de medicamente de care beneficiază asiguraţii în cadrul programelor naţionale. În acest caz, vorbim de programul naţional pentru amiotrofia spinală musculară”, a explicat pentru news.ro Răzvan Mihai Prisada, directorul ANMDMR.
Criteriile de siguranţă şi eficacitate, îndeplinite de noua terapie genică Zolgensma, aprobată în 2019 în SUA iar în 2020 în Uniunea Europeană. Directorul ANM, despre rambursarea costului terapiei: „Există o intenţie de a intra într-un protocol de colaborare cu CNAS”.
„Acordarea acelui punctaj are la bază mai multe criterii, unele dintre ele sunt legate de evaluările care au fost făcute apropo de siguranţă şi eficacitate de către agenţiile din ţările pe care le-am menţionat, alte puncte ţin de statutul respectivului medicament. Evident decizia finală trebuie să ţină cont de aceste criterii care sunt legate de eficacitate şi de siguranţă.
Din ceea ce ştim, în acest moment sunt 8 ţări în Europa care au acest medicament în listele medicamentelor de care beneficiază asiguraţii, există condiţii probabil separate, diferite, nu ştiu foarte multe despre sistemele de rambursare, uneori aceste lucruri sunt netransparente.
Cu siguranţă au existat, am fost informaţi de către colegii de la CNAS, au existat discuţii între CNAS şi deţinătorul de autorizaţie de punere pe piaţă pentru acest medicament şi există o intenţie de a intra într-un protocol de colaborare cu CNAS.
Prisada:” Modul clasic în care am privit inovaţia se schimbă, trebuie să ne adaptăm„
"Din punctul Agenţiei de vedere, dacă există şi se identifică sursele de finanţare necesare, acest lucru ar putea să se întâmple în acest an. Eu tot încerc să spun şi o să spun de acum în colo mai des, de acum în colo trebuie să ne aşteptăm la din ce în ce mai multe terapii de acest gen. Modul clasic în care am privit inovaţia se schimbă. Sunt altceva, sunt clase noi de terapii, trebuie să ne adaptăm, este un lucru pe care l-am mai discutat şi cu colegii din alte ţări, evoluţia a fost destul de rapidă şi trebuie cu toţii să găsim căi de a ne adapta, inclusiv modalitatea de evaluare a acestor noi terapii”, a explicat Răzvan Prisada.
Dr. Andrada Mirea, medic specialist pediatrie la Centrul Naţional Clinic de Recuperare Neuropsihomotorie Copii „Dr. Nicolae Robănescu” din Bucureşti, a relatat pentru News.ro experienţa pe care a avut-o până acum cu această nouă terapie. Expertul spune că încă nu există oficial în România protocol de administrare pentru acest medicament şi că acest lucru va trebui făcut.
„Nu este încă stabilit protocolul de administrare la nivelul ţării noastre, dar vă pot spune din experienţa ţărilor din Occident SUA, de exemplu, a acceptat ca acest medicament să fie administrat doar până la vârsta de doi ani, excepţional în anumite cazuri se face şi peste această vârstă, iar în Europa, în prospectul aşa cum este aprobat de EMA ( Agenţia Europeană a Medicamentului) este stipulată greutatea de 21 de kilograme ca fiind o limită a administrării acestui medicament. Din experienţa clinicilor din Europa, totuşi, se tinde spre greutăţi mai mici şi în general se impune o limită de vârstă vis a vis de reacţiile adverse, dar cu toţii ştim că profesia aceasta de medic este una liberală şi dacă nu există condiţii impuse de stat printr-un anumit protocol de program naţional, dacă se fac strângeri de fonduri, atunci totul ţine de decizia medicului şi de hotărârea acestuia, de tot ce înseamnă experienţa sa în acest domeniu şi în privinţa acestui medicament.
Dacă vorbim despre acest tratament acordat prin rambursare de către statul român ( n.red. medicul face referire la Zolgensma, tratament încă nerambursat de stat), medicul va decide ţinând cont de protocolul care încă nu există deci nu ştim exact ce va include ca şi reguli şi ca şi condiţii acest protocol.
Unii au primit tratamentul prin intermediul acelei tombole, practic un program de uz compasional de ultimă instanţă iar alţii au primit tratamentul prin strângeri de fonduri, în total sunt 9 pacienţi pe care i-am avut în evidenţă”, a explicat medicul.
Dr. Mirea: „În cazul pacientului care a primit doar Zolgensma, boala a stagnat, nu au mai murit neuronii, copilul a putut evolua din punct de vedere motor”.
„Cu excepţia unui singur pacient care în urma administrării Zolgensma nu a mai primit alt tratament, de acela vă pot spune că are efecte ca şi la Spinraza,(n.red, un alt medicament destinat amiotrofiei spinale, decontat de stat) efecte care arată că boala a stagnat, că nu au mai murit neuronii şi copilul a putut să evolueze din punct de vedere motor, toţi ceilalţi au primit în continuare tratamentul rambursat de statul român ( Spinraza) şi atunci nu vă pot spune dacă Zolgensma în sine i-a ajutat sau celălalt sau împreună.
Este important că experienţa şi cunoaşterea din studiile clinice legate de pacienţii trataţi doar cu acest tip de tratament, acestea sunt cele care îşi spun cuvântul. Noi avem o experienţă limitată de faptul că primesc două tratamente şi atunci nu poţi să spui care acţionează.“
Legea 190 din 2018, la articolul 7, menţionează că activitatea jurnalistică este exonerată de la unele prevederi ale Regulamentului GDPR, dacă se păstrează un echilibru între libertatea de exprimare şi protecţia datelor cu caracter personal.

 13.4° Constanța
13.4° Constanța 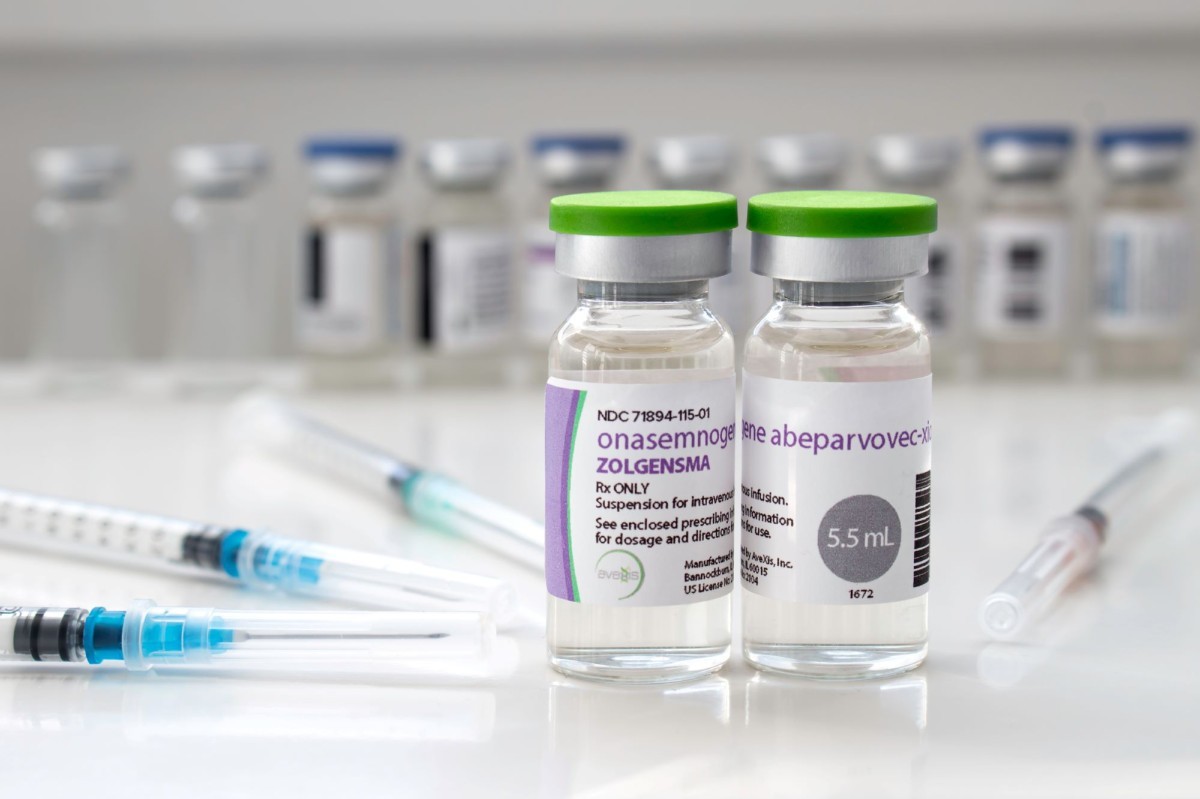












.jpg_t.jpg)